Le syndrome de la queue de cheval est une atteinte neurologique rare mais grave, causée par une compression aiguë ou subaiguë des racines nerveuses caudales au niveau du cône terminal de la moelle épinière. Sa prévalence est estimée à environ 1 personne sur 30 000 à 100 000 par an, avec une prédominance chez les adultes de 30 à 49 ans. Le délai de prise en charge est un facteur pronostique déterminant : toute suspicion impose une évaluation en urgence, car un retard de diagnostic peut entraîner des séquelles irréversibles, notamment sphinctériennes et motrices (1).
Anatomie de la queue de cheval
La queue de cheval correspond à un ensemble de nerfs et de racines nerveuses provenant de l’extrémité distale de la moelle épinière, issue des segments lombaires, sacrés et coccygiens. Ces racines nerveuses descendent dans le canal rachidien au-delà du cône médullaire, généralement situé à la jonction L1-L2. Ces racines nerveuses assurent :
- L’innervation motrice et sensitive des membres inférieurs.
- L’innervation sensitive de la région périnéale.
- Le contrôle volontaire des sphincters urinaires et anaux.
La compression de ces racines nerveuses entraîne des perturbations fonctionnelles graves, en particulier aux niveaux L3-L5 (1, 2).
L’anatomie de la queue de cheval, en particulier la partie proximale, est hypovasculaire, la rendant particulièrement vulnérable en cas de compression. Les racines de la queue de cheval ont à la fois une racine dorsale et ventrale. La racine ventrale fournit des fibres motrices pour la voie efférente ainsi que des fibres sympathiques. La racine dorsale est composée de fibres afférentes pour la transmission de la sensation (3).
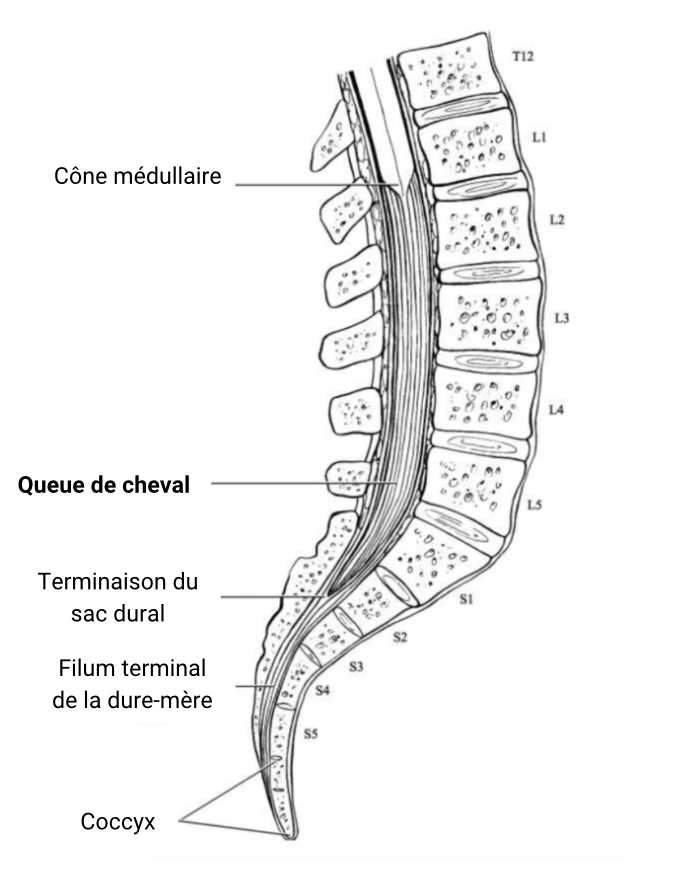
Schéma traduit par Neuroxtrain
Étiologie
La compression des racines nerveuses peut résulter de plusieurs causes, parmi lesquelles :
- Hernie discale lombaire : la cause principale du syndrome de la queue de cheval, dans 45 à 70% des cas, souvent aux niveaux L4-L5 et L5-S1 (2, 6)
- Sténose lombaire
- Tumeurs intraspinales, telles que les méningiomes ou les neurinomes (2).
- Infections rachidiennes, notamment les abcès épiduraux ou les spondylodiscites (4).
- Traumatismes rachidiens, notamment les fractures ou luxations avec compression du canal rachidien (5).
- Hématomes épiduraux, spontanés ou post-chirurgicaux.
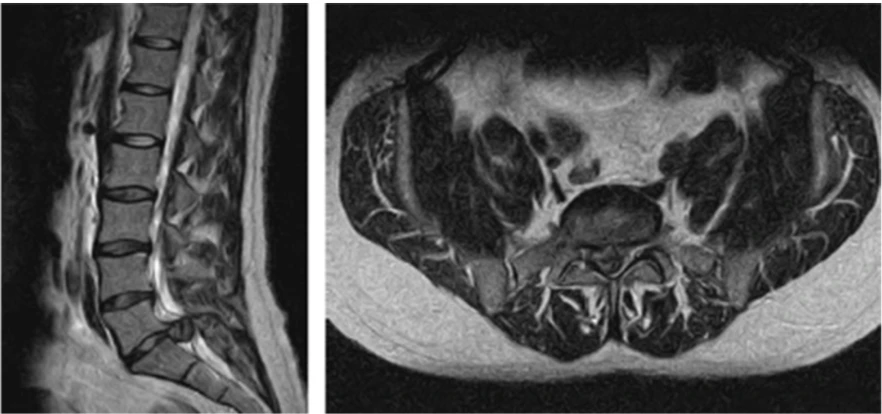
Exemple d'IRM d'une hernie discale provoquant une compression de la queue de cheval. L'image sagittale de gauche montre une hernie discale postérieure au niveau L5/S1, et l'image axiale de droite au niveau L5/S1 montre que la hernie discale remplit presque tout le canal rachidien et comprime la queue de cheval. Crédits image : Article de Lavy et al. 2022.
Manifestations cliniques
Les signes cliniques du syndrome de la queue de cheval incluent trois manifestations majeures, bien qu'elles ne soient pas toujours présentes simultanément :
1. Douleurs lombaires sévères avec irradiation radiculaire dans un ou deux membres inférieurs.
2. Déficits neurologiques des membres inférieurs :
o Faiblesse motrice, souvent asymétrique, pouvant évoluer vers une parésie ou une paralysie.
o Troubles sensitifs : hypoesthésie, paresthésies, voire anesthésie dans les territoires radiculaires concernés.
o Les réflexes tendineux sont généralement diminués ou absents, reflétant une atteinte des nerfs périphériques.
3. Troubles sphinctériens et périnéaux :
o Altération de la fonction vésicale : difficulté à uriner, changement de jet, incontinence et rétention, dues à la perturbation des fibres autonomes.
o Perte du tonus anal : dysfonctionnement intestinal tel que la constipation, l'incontinence, l'incapacité à contrôler les mouvements, l’absence de perception du besoin d’évacuation.
o Anesthésie de selle ou diminution de la sensation dans le périnée : présent chez jusqu’à 93% des patients (2).
o Dysfonctionnement sexuel (1,3,4)
Les troubles sphinctériens représentent un signe de gravité majeur, nécessitant une prise en charge neurochirurgicale immédiate pour éviter des séquelles irréversibles (3).

L’étude récente de Liu et al souligne l’importance de considérer le syndrome de queue de cheval chez les patients présentant une dysfonction urinaire isolée, en particulier après une chirurgie lombaire, même en l’absence de symptômes neurologiques typiques. Leur étude présente le cas d’un homme de 46 ans ayant développé un syndrome de la queue de cheval après une microdiscectomie lombaire. Contrairement aux manifestations classiques, ce patient ne présentait que des symptômes urinaires, notamment une rétention urinaire, sans perte sensorielle périnéale ni déficits neurologiques des membres inférieurs. Cette présentation atypique a conduit à un retard diagnostique, les symptômes initiaux étant attribués à des complications urinaires postopératoires courantes. Ce n'est qu'au septième jour postopératoire qu'une IRM a révélé un hématome épidural spinal, nécessitant une évacuation chirurgicale d'urgence. Malgré ce retard, le patient a récupéré complètement ses fonctions neurologiques, avec une restauration des fonctions vésicales et intestinales trois mois après l'intervention (5).
Diagnostic
Le diagnostic clinique repose sur l’identification des symptômes évoqués, nécessitant une évaluation neurologique complète (force musculaire, réflexes ostéotendineux, sensibilité périnéale, tonus anal).
L’imagerie de choix est l’IRM lombaire en urgence, gold standard pour confirmer la compression des racines nerveuses (6). En cas de contre-indication à l’IRM, un scanner lombaire peut être envisagé, bien qu’il soit moins sensible pour les tissus mous.
Prise en charge
Une consultation neurochirurgicale ou orthopédique rapide est essentielle. Le type d’intervention dépend de l’étiologie sous-jacente : discectomie en cas de hernie discale, laminectomie pour une sténose sévère, ou drainage en cas d’abcès épidural (1,4). En cas de suspicion d’infection rachidienne, une antibiothérapie est également mise en place.
Rôle du kinésithérapeute
En tant que kinésithérapeute, nous sommes souvent en première ligne pour le traitement des lombalgies et sciatalgies. Il faut être vigilant face aux signes d’alerte du syndrome. Si des symptômes suggestifs apparaissent (troubles sphinctériens, anesthésie en selle, déficit moteur aigu), une orientation immédiate vers un service d’urgence est nécessaire pour un examen médical approfondi (3).
Rééducation post-opératoire
La rééducation post-opératoire vise à restaurer les fonctions motrices, sensitives et sphinctériennes. Elle comprend :
Rééducation motrice : La restauration de la mobilité et de la force musculaire des membres inférieurs est essentielle. Des exercices de renforcement musculaire, en particulier pour les quadriceps, les ischio-jambiers et les muscles fessiers, sont souvent prescrits pour améliorer la stabilité et la fonction des jambes (3, 6). La rééducation de la marche est également primordiale, en particulier après une période prolongée d'immobilité.
Rééducation sphinctérienne : En raison de l'impact du syndrome sur les sphincters, la rééducation périnéale est un élément clé du programme de rééducation. Des techniques de renforcement du plancher pelvien et des exercices de biofeedback peuvent améliorer le contrôle sphinctérien, particulièrement pour les patients présentant une incontinence urinaire ou fécale résiduelle (4, 6).
Gestion des douleurs résiduelles : Les techniques non médicamenteuses, telles que l'électrothérapie et les mobilisations douces, sont couramment utilisées pour gérer la douleur résiduelle (5). L'utilisation de la chaleur, du froid, ainsi que des techniques manuelles peut également jouer un rôle dans le soulagement des douleurs chroniques et la réduction de la raideur musculaire post-chirurgicale (4).
Éducation thérapeutique : L'éducation des patients sur l'importance de l’adoption de techniques adaptées dans la vie quotidienne est essentielle pour prévenir les récidives et améliorer la qualité de vie (3). Les patients doivent également être informés des signes d'alerte d’une récidive ou d’une complication, ce qui permet de réagir rapidement en cas de symptômes inquiétants.
Suivi à long terme : Une réévaluation régulière des progrès et une réadaptation continue sont nécessaires pour maintenir et améliorer les gains fonctionnels à long terme (4). Les patients doivent être suivis pendant plusieurs mois, voire années, pour surveiller les progrès fonctionnels et la gestion des symptômes résiduels (6).
Tout le contenu de cet article est présenté à titre informatif. Il ne remplace en aucun cas l’avis ou la visite d’un professionnel de santé.
Sources
1. Rider LS, Marra EM. Cauda Equina and Conus Medullaris Syndromes. [Updated 2023 Aug 7]. In: StatPearls [Internet].
2.Woodfield, J., Lammy, S., Jamjoom, A. A. B., Fadelalla, M. A. G., Copley, P. C., Arora, M., Glasmacher, S. A., Abdelsadg, M., Scicluna, G., Poon, M. T. C., Pronin, S., Leung, A. H. C., Darwish, S., Demetriades, A. K., Brown, J., Eames, N., Statham, P. F. X., Hoeritzauer, I., UCES Study Collaborators, & British Neurosurgical Trainee Research Collaborative (2022). Demographics of Cauda Equina Syndrome: A Population-Based Incidence Study. Neuroepidemiology, 56(6), 460–468. Article sous Creative Commons Licence CC BY 4.0
3.Wang, Q., Hou, G., Wen, M., Ren, Z., Duan, W., Lei, X., Yao, Z., Zhao, S., Ye, B., Tu, Z., Huang, P., Xie, F., Gao, B., Hu, X., & Luo, Z. (2024). How to assess the long-term recovery outcomes of patients with cauda equina syndrome before surgery: a retrospective cohort study. International journal of surgery (London, England), 110(7), 4197–4207. Article sous Creative Commons Licence CC BY
4.Srikandarajah, N., Wilby, M., Clark, S., Noble, A., Williamson, P., & Marson, T. (2018). Outcomes Reported After Surgery for Cauda Equina Syndrome: A Systematic Literature Review. Spine, 43(17), E1005–E1013. Article sous Creative Commons Licence CC BY
5.Liu, G., Li, Q., Ruan, H., Zhu, B., Ma, W., & Hu, Y. (2025). Cauda Equina Syndrome Without Perineal Sensory Changes or Lower Extremity Neurological Deficits Following Postoperative Spinal Epidural Hematoma: A Case Report and Literature Review. Orthopaedic surgery, 17(2), 653–659. Article sous Creative Commons Licence CC BY
6.Lavy, C., Marks, P., Dangas, K., & Todd, N. (2022). Cauda equina syndrome-a practical guide to definition and classification. International orthopaedics, 46(2), 165–169. Article sous Creative Commons Licence CC BY